
El papel de CRISPR en la ingeniería del microbioma [Podcast]
El papel de CRISPR en los avances científicos en la ingeniería del microbioma
Se descubrieron por primera vez repeticiones palindrómicas cortas agrupadas regularmente interespaciadas (CRISPR) en el genoma de bacterias marinas. Cuando se enfrentó a una amenaza viral, las células bacterianas desarrollaron una respuesta inmunitaria al capturar y copiar fragmentos de ADN de virus. Esto permitió a las bacterias reconocer ataques posteriores y escindir el ADN viral para detener la infección viral. También se descubrió que la enzima Cas era responsable de la escisión del ADN. Este mecanismo de defensa fue aprovechado posteriormente por Doudna y Charpentier, que podían dirigirse a una secuencia de ADN específica y aislarla utilizando el sistema CRISPR-Cas9 (1).
Durante la última década, CRISPR-Cas9 ha demostrado ser inmensamente valioso en el descubrimiento y la fabricación de fármacos. Con un ARN guía sintético (ARNg), los científicos pueden dirigirse a una secuencia de ADN específica y emplear Cas9 para cortarla. Posteriormente, la maquinaria de reparación del huésped intenta reparar el ADN a través de una unión final no homóloga (NHEJ), lo que provoca mutaciones aleatorias que alteran la función génica. Mediante este mecanismo, los científicos ahora podrían silenciar los genes para esclarecer su papel en el fenotipo de la enfermedad, lo que puede beneficiar al descubrimiento de objetivos. Además, los científicos también pueden utilizar CRISPR-Cas9 para desentrañar los mecanismos de resistencia a los fármacos mediante la identificación del conjunto de genes asociados con la evasión del sistema inmunitario.
Sin embargo, hoy exploraremos una aplicación diferente de CRISPR: ingeniería del microbioma. Presentado por Molecular Devices, el reciente episodio del podcast Drug Target Reviews analiza las aplicaciones de CRISPR en la ingeniería del microbioma y cómo puede superar el cuello de botella de la investigación del microbioma humano.
Únase a los expertos líderes, el Dr. Jakob Haaber, vicepresidente y director de tecnologías de entrega, SNIPR Biome y el Dr. Richard Fox, cofundador, director ejecutivo y director de tecnología de Infinome Biosciences, mientras analizan la amplia gama de usos para CRISPR, incluidos los tratamientos y la biofabricación.
Cómo ayuda CRISPR-Cas9 a explorar el papel del microbioma humano en las enfermedades
Ahora se sabe bien que el cuerpo humano contiene billones de microorganismos, superando así a las células humanas. Estos microorganismos, denominados de forma colectiva el microbioma, forman una simbiosis con el organismo mediante la regulación del entorno extracelular y la protección de las células contra los patógenos. Por lo tanto, no es de extrañar que las alteraciones en el microbioma estén estrechamente asociadas con numerosas enfermedades, desde la diabetes y la obesidad hasta el cáncer.
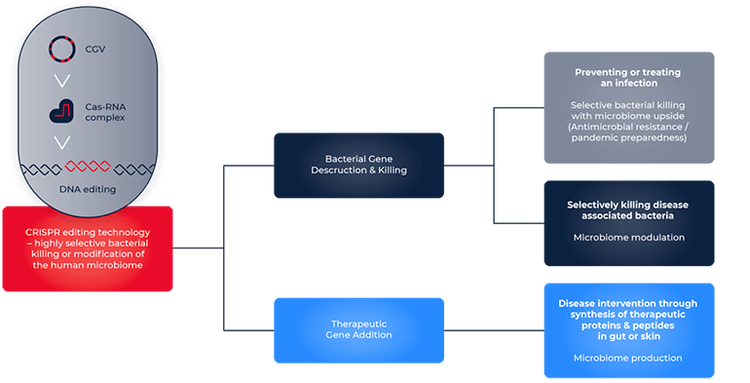
Ventajas de CRISPR y desarrollos recientes
Según Richard Fox, cofundador, CEO y CTO de Infinome Biosciences, la principal fortaleza de CRISPR proviene de su capacidad para ampliar la edición del genoma. “En lugar de mutaciones aleatorias en un pequeño conjunto de genes diana, ahora podemos editar con precisión una vía o genoma completo, introduciendo cientos de miles de cambios”.
La edición del genoma a gran escala da lugar a bibliotecas celulares disponibles comercialmente que los investigadores pueden integrar en un cribado fenotípico de alto rendimiento. Estas bibliotecas eliminan la necesidad de eliminar manualmente un gran número de genes para la elaboración de perfiles fenotípicos y proponen una solución para la aceleración de estudios de descubrimiento de fármacos.
Otra ventaja de las tecnologías CRISPR es la especificidad mejorada. La edición de genes del microbioma es uno de los campos que aprovecha los beneficios de la especificidad. Los sistemas CRISPR se pueden programar para cortar ADN bacteriano específico o incluso eliminar circuitos genéticos dentro de las paredes celulares bacterianas sin destruir la célula. En conjunto, estos avances impulsan nuevas terapias génicas para las desviaciones de la microbiota intestinal.
Mientras tanto, los sistemas CRISPR han permitido la fabricación de construcciones genéticas más pequeñas para facilitar el envasado en vehículos de entrega. Por lo tanto, el vehículo de suministro puede transportar múltiples componentes además de CRISPR, lo que constituye un tratamiento basado en genes multifuncional que logra mucho más que simplemente cortar o insertar ADN.
Aceleración en la fabricación de tecnologías CRISPR
La brecha entre la biología sintética y la bioingeniería suele deberse a problemas relacionados con el tiempo y el coste. La comercialización de una solución de biofabricación requiere grandes entidades con una infraestructura bien construida, automatización robusta, mucha gente, instrumentación, informática y mucho capital. Por lo tanto, no es sorprendente que el desarrollo de productos biológicos pueda llevar 5de a10 años y muchos millones de dólares. Se trata de una inversión bastante arriesgada, por lo que las empresas farmacéuticas a menudo dudan en participar en ella, dejando territorios con un enorme potencial terapéutico sin explorar.
La configuración del sistema de edición del genoma habilitado para CRISPR es uno de los cuellos de botella en los flujos de trabajo. El diseño de sistemas de ingeniería del genoma a gran escala es bastante laborioso porque es posible que se necesiten producir cantidades diminutas de secuencia del donante para dirigirse y editar con precisión 10 000 loci en un genoma completo.
Uno de los cofundadores de Infinome Biosciences, Andrew Garst, ideó una innovación clave al emparejar la secuencia guía que dirige el corte con la secuencia del donante que media en la reparación, reduciendo así la edición del genoma ancho a solo unos pocos clics. Richard Fox cree que “dichos sistemas automatizados de diseño y construcción pueden crear bibliotecas de células editadas en menos de una semana, lo que es la fracción del esfuerzo que solía requerir”.
Pasos de la edición de genes microbianos
El primer paso en la edición de genes para el microbioma intestinal es la validación in vitro del sistema CRISPR. La especificidad de la edición CRISPR se analiza frente a un conjunto de paneles bacterianos representativos del microbioma intestinal. El objetivo es garantizar que el sistema CRISPR se dirija a una subespecie predeterminada de bacterias y que las bacterias beneficiosas estén exentas de la edición genética inducida por CRISPR
A continuación, la validación continúa con los estudios preclínicos y clínicos. Mediante técnicas de secuenciación del genoma, los investigadores demuestran que la edición de genes no afecta al microbioma de forma dañina. Por supuesto, los efectos fuera del objetivo podrían ocurrir inevitablemente, como se revela mediante secuenciación del genoma completo. El curso de acción es supervisar la tasa de aparición y garantizar que estos efectos sean triviales y no interfieran con la edición génica.
La secuenciación y el perfil fenotípico revelan el conjunto de ediciones que lleva un genoma, así como las cepas predominantes en una población bacteriana. Para validar aún más el éxito de la edición dirigida del genoma, se puede someter a la población bacteriana a factores de estrés ambiental y supervisar su comportamiento. Esto garantiza que la edición génica confiere a las bacterias las propiedades deseadas, por ejemplo, la capacidad de crecer bajo un estrés ambiental como la hipoxia.

Con los flujos de trabajo acelerados de CRISPR, los investigadores pueden obtener el conjunto de ediciones de genes beneficiosos entre cientos de miles de genes knockout.
Los sistemas CRISPR también liberan la flexibilidad de enriquecer o agotar la misma cepa bacteriana dependiendo de la necesidad específica de la investigación. Por ejemplo, los investigadores de Infinome implementaron CRISPR para diseñar cepas de E. coli para aumentar la producción de lisina, un aminoácido crítico utilizado como aditivo alimentario. Por otro lado, SNIPR utilizó el mismo sistema para erradicar las cepas perjudiciales de E. coli del intestino de los pacientes con cáncer hematológico para prevenir las infecciones del torrente sanguíneo.
Mirando hacia el futuro de CRISPR
Como se mencionó anteriormente, CRISPR potencia la lucha contra las bacterias patógenas. Se ha demostrado varias veces que los tratamientos antibióticos convencionales alteran la microbiota intestinal al actuar sobre bacterias dañinas y beneficiosas. CRISPR puede ayudar a mejorar la especificidad de las bacterias para mantener el equilibrio de la microbiota intestinal humana.
Otra perspectiva interesante impulsada por CRISPR es la capacidad de diseñar cepas bacterianas con potencial terapéutico. Esto se puede utilizar para añadir funciones genéticas al microbioma a través de bacterias modificadas genéticamente, que pueden expresar una enzima o metabolito específico que el organismo carecía anteriormente.
Por último, la implementación exitosa de CRISPR en ingeniería biomédica y bioindustrial se basa en la capacidad de realizar ediciones combinatorias, también conocidas como “complicación del ADN”. Especialmente en sistemas microbianos grandes, la capacidad de introducir múltiples ediciones para reducir el número de rondas de cribado será primordial para implementar la producción bioindustrial.
Molecular Devices ayuda a los científicos proporcionando tecnologías de vanguardia que aceleran el objetivo inmediato de la edición del genoma de CRISPR-Cas9. Un cribado preciso de la biblioteca y una selección de los éxitos editados por CRISPR es clave en los flujos de trabajo de ingeniería del microbioma, lo que permite una disponibilidad más rápida del producto de biofabricación en el mercado.
- Doudna, Jennifer A. y Emmanuelle Charpentier. “La nueva frontera de la ingeniería genómica con CRISPR-Cas9”. Ciencia 346,6213 ( 2014): 1258096.
CRISPR在微生物组工程科学突破中的作用
CRISPR首次在海洋细菌的基因组中发现,当面临病毒威胁时,细菌细胞通过捕获和复制病毒的DNA片段来产生免疫反应,这使得细菌能够识别随后的攻击并切割病毒DNA以阻止病毒感染。另外,还发现Cas酶负责切割DNA,这种防御机制后来被Doudna和Charpentier利用,他们可以靶向目标DNA序列,并使用CRISPR-Cas9系统将其分离(1)。
在过去的十年中,CRISPR-Cas9已被证明在药物发现和药物制造中具有巨大的价值。使用合成向导RNA(gRNA),科学家可以靶向目标DNA序列并使用Cas9进行切割。随后,宿主修复机制试图通过非同源末端连接(NHEJ)修复DNA,导致改变基因功能的随机突变。利用这种机制,科学家们现在可以使基因沉默来阐明它们在疾病表型中的作用,这有利于发现目标。此外,科学家还可以利用CRISPR-Cas9,通过识别与免疫系统逃避相关的一组基因来揭示耐药机制。
然而,今天,我们将探索CRISPR的不同应用:微生物组工程。本期内容我们来讨论CRISPR在微生物组工程中的应用以及它如何克服人类微生物组研究的瓶颈。
本次嘉宾:Jakob Haaber博士,副总裁兼交付技术主管SNIPR Biome和Infinome Biosciences联合创始人、CEO 兼CTO Richard Fox博士一起探讨CRISPR的广泛用途,包括治疗和生物制造。
CRISPR-Cas9如何帮助探索人类微生物组在疾病中的作用
众所周知,人体含有数万亿种微生物,在数量上超过了人体细胞。这些微生物统称为微生物组,通过调节细胞外环境和保护细胞免受病原体侵害,与人体形成共生关系。因此,从糖尿病、肥胖到癌症,微生物组的破坏与许多疾病密切相关也就不足为奇了。

通过设计CRISPR-Cas9系统来切割特定的细菌DNA序列以消除致病细菌,这种特异性使CRISPR技术减轻对整体微生物组的破坏,实现药物发现进程的加速。。SNIPR Biome是积极致力于实现这一目标的公司之一,SNIPR Biome副总裁兼CRISPR负责人和交付技术主管Jakob Haaber博士描述了CRISPR在致病性大肠杆菌消除中的应用:“我们使用CRISPR杀死大肠杆菌。目前,治疗细菌感染最常用的就是抗生素。但抗生素耐药性的发生率增加,进而使抗生素无效。CRISPR的优点是它不区分抗生素敏感和抗生素耐药细菌。他还建议,CRISPR可以专门针对致病细菌,而不影响健康肠道微生物组中不可或缺的有益细菌,而不是像抗生素一样,对健康细菌和病原体都有影响。
CRISPR的优势和近年发展

Infinome Biosciences的联合创始人、CEO兼CTO Richard Fox表示,CRISPR的主要优势在于其扩大基因组编辑的能力。“我们现在可以精确地编辑整个通路或基因组,而不是一小部分目标基因上的随机突变,从而引入数十万个变化。
大规模的基因组编辑产生可商用的细胞库,研究人员可以将其整合到高通量表型筛选中。这些库消除了手动敲除大量基因进行表型分析的需要,并为加速药物发现研究提出了解决方案。
CRISPR技术的另一个优点是提高了特异性,微生物组基因编辑是受益于特异性的领域之一。CRISPR系统可以被编程为切割特定的细菌DNA,甚至在不杀死细胞的情况下去除细菌细胞壁内的基因回路。综上所述,这些进步推动了肠道微生物群偏差的新基因疗法。
与此同时,CRISPR系统已经能够制造出更小的基因构建体,以便更容易地装配到递送载体中。因此,除了CRISPR之外,递送载体还可以携带多种成分,构成一种多功能的基于基因的疗法,不仅仅是切割或插入DNA。
加速CRISPR技术的制造
合成生物学和生物工程之间的差距通常是由时间和成本问题引起的。将生物制造解决方案推向市场需要大型实体,这些实体具有完善的基础设施、强大的自动化、大量的人员、仪器、信息学和大量资金。因此,生物制剂的开发可能需要5-10年和数百万美元也就不足为奇了。这是一项风险相当大的投资,因此制药公司往往不愿参与其中,从而一些具有巨大治疗潜力的领域未得到开发。
支持CRISPR的基因组编辑系统的设置是工作流程的瓶颈之一。大规模基因组工程系统的设计非常费力,因为需要产生微量的供体序列来靶向并精确地将10,000个位点编辑到整个基因组。
Infinome Biosciences的联合创始人之一Andrew Garst提出了一项关键创新,将指导切割的引导序列与介导修复的供体序列配对,从而将广基因组编辑减少到只需点击几下。Richard Fox认为,“这种自动化设计和构建系统可以在不到一周的时间内创建编辑过的细胞库,这是过去所花费的努力的一小部分”。
微生物基因编辑步骤
肠道微生物组基因编辑的第一步是CRISPR系统的体外验证。CRISPR编辑的特异性是针对一组代表肠道微生物组的细菌进行测试的,以确保CRISPR系统针对预定的细菌亚种,并且使得有益细菌不受CRISPR诱导的基因编辑的影响。
然后,验证继续进行到临床前和临床研究。利用基因组测序技术,研究人员证明基因编辑不会以有害的方式扰乱微生物组。当然,脱靶效应不可避免地会发生,正如全基因组测序所揭示的那样。我们需要做是监测发生率,并确保这些影响是微不足道的,不会干扰基因编辑。
测序和表型分析揭示了基因组携带的一组编辑以及细菌种群中的主要菌株。为了进一步验证靶向基因组编辑的成功,可以将细菌种群置于环境压力源中并监测其行为。这确保了基因编辑赋予细菌所需的特性,例如在缺氧等环境压力下生长的能力。

通过加速的CRISPR工作流程,研究人员可以在数十万个基因敲除中得到一组有益的基因编辑。
CRISPR系统还可以根据特定的研究需求,灵活地富集或消耗相同的细菌菌株。例如,Infinome的研究人员应用CRISPR来设计大肠杆菌菌株,以扩大赖氨酸的生产,赖氨酸是一种用作食品添加剂的关键氨基酸。另一方面,SNIPR使用相同的系统从血液癌患者的肠道中根除有害的大肠杆菌菌株,以防止血液感染。
展望
如前所述,CRISPR能够对抗致病菌,已多次证明,传统的抗生素治疗通过作用有害和有益细菌来破坏肠道微生物群。CRISPR可以帮助增强细菌的特异性,以维持人类肠道微生物群的平衡。
另一个令人兴奋的前景是设计具有治疗潜力的细菌菌株的能力。这可用于通过工程细菌为微生物组添加遗传功能,这些细菌可以表达身体以前缺乏的特定酶或代谢物。
最后,CRISPR在生物医学和生物工业工程中的成功应用依赖于进行组合编辑的能力,也称为“DNA洗牌”。特别是在大型微生物系统中,引入多次编辑以减少筛选轮次的能力对于生物工业生产至关重要。
Molecular Devices通过提供前沿技术来帮助科学家加速CRISPR-Cas9基因组编辑的近期目标。准确的文库筛选和CRISPR编辑命中物的选择是微生物组工程工作流程的关键,使生物制造产品更快地推向市场。
1. Doudna, Jennifer A.和Emmanuelle Charpentier。“CRISPR-Cas9基因组工程的新前沿。科学346,6213(2014):1258096。