
Evolución del papel de las células CHO en el desarrollo de líneas celulares
Desde la primera aprobación de la insulina recombinante y de la hormona de crecimiento humana a principios de la década de 1980, las entidades regulatorias han autorizado una gran cantidad de productos terapéuticos de las proteínas recombinantes, en especial, la FDA en EE. UU. y la EMA en Europa. Dado este aumento significativo en la introducción exitosa de agentes terapéuticos biológicos, existe una necesidad crucial en el espacio de detección de fármacos para apoyar procesos de fabricación más eficientes que requieran líneas celulares altamente productivas.
Las células del ovario de hámster chino (CHO) son una línea celular similar a un epitelio muy susceptible a la transfección y han surgido como el estándar de referencia para la fabricación de proteínas terapéuticas aprobadas.
¿Por qué se utilizan las celdas CHO?
Varias propiedades clave de las células CHO han impulsado su establecimiento como la línea celular huésped preferida para la aprobación regulatoria de productos terapéuticos recombinantes:
1
Adaptable al crecimiento en el cultivo de la suspensión, que es ideal para la producción a gran escala en biorreactores
2
Adaptable al crecimiento en suplementos de medios sin sérum y definidos químicamente (sin animales), lo que garantiza la reproducibilidad entre diferentes lote de cultivos celulares
3
Permita modificaciones postraduccionales (p. ej., glicosilaciones) a las proteínas recombinantes que sean compatibles y bioactivas en los humanos
4
Se han desarrollado varios sistemas de selección química y amplificación génica para las células CHO, optimizados para un mayor rendimiento de la proteína recombinante por célula.
Historial de celdas CHO
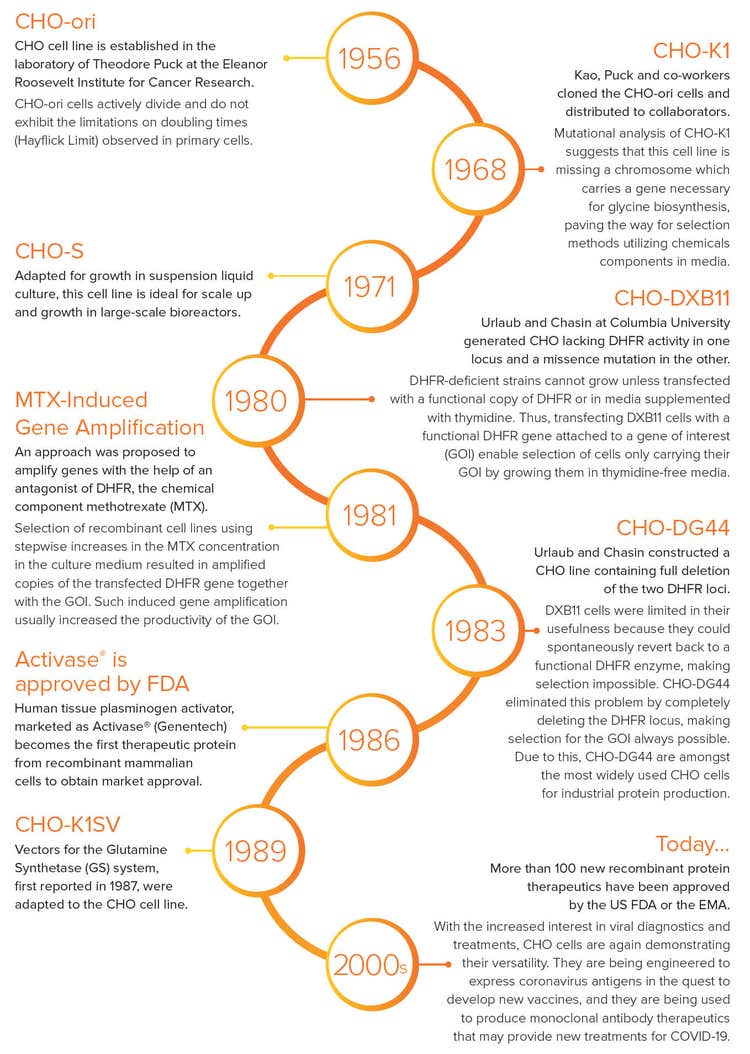
1956 - Células CHO-ori
La línea celular CHO se establece en el laboratorio de Theodore Puck en el Instituto Eleanor Roosevelt para la Investigación del Cáncer. Las células CHO-ori se dividen de forma activa y no muestran las limitaciones en los tiempos de duplicación (límite de Hayflick) observados en las células primarias.
1968 - Células CHO-K1
Kao, Puck y sus colaboradores clonaron las células CHO-ori y las distribuyeron a los colaboradores. El análisis de las variables de CHO-K1 sugiere que a esta línea celular le falta un cromosoma que porta un gen necesario para la biosíntesis de la glicina, lo que allana el camino para los métodos de selección que utilizan componentes CHO-S de productos químicos en los medios.
1971 - Células CHO-S
Adaptada para el crecimiento en el cultivo líquido en suspensión, esta línea celular es ideal para escalar y crecimiento en biorreactores a gran escala.
1980 - Células CHO-DXB11
Urlaub y Chasin de la Universidad de Columbia generaron CHO sin actividad de DHFR en un locus y una mutación de falta en el otro. Las cepas deficientes en DHFR no pueden crecer a menos que se transfecten con una copia funcional de DHFR o en medios suplementados con timidina. Por lo tanto, la transfectación de las células DXB11 con un gen DHFR funcional unido a un gen de interés (GOI) permite la selección de células que solo transportan su GOI haciéndolas crecer en medios libres de timidina.
1981 - Amplificación de gen inducida por MTX
Se propuso un enfoque para amplificar los genes con la ayuda de un antagonista de DHFR, el componente químico de metotrexato (MTX). La selección de líneas celulares recombinantes utilizando aumentos escalonados en la concentración de MTX en el medio de cultivo dio lugar a copias amplificadas del gen DHFR transfectado junto con el GOI. Tal amplificación génica inducida generalmente aumentó la productividad del GOI.
1983 - Células CHO-DG44
Urlaub y Chasin construyeron una línea CHO que contiene la eliminación completa de los dos loci DHFR. Las células DXB11 se vieron limitadas en su utilidad porque podían volver de forma espontánea a una enzima DHFR funcional, haciendo imposible la selección. CHO-DG44 eliminó este problema eliminando por completo el locus DHFR, haciendo siempre posible la selección para el GOI. Debido a esto, CHO-DG44 se encuentra entre las células CHO más utilizadas para la producción de proteínas industriales.
1986 - Activase® está aprobado por la FDA
El activador del plasminógeno de tejido humano, comercializado como Activase® (Genentech) se convierte en la primera proteína terapéutica de las células de mamífero recombinantes para obtener la aprobación de comercialización.
1989 - Células CHO-K1SV
Los vectores para el sistema de la sintetasa de laglutamina (GS), notificados por primera vez en 1987, se adaptaron a la línea celular CHO.
2000 - Hoy...
La FDA de los EE. UU. o la EMA han aprobado más de 100 nuevos agentes terapéuticos de las proteínas recombinantes.
Con el mayor interés en el diagnóstico y los tratamientos víricos, las células CHO están demostrando de nuevo su versatilidad. Se están diseñando para expresando los antígenos del coronavirus en la búsqueda de desarrollar nuevas vacunas y se están utilizando para producir agentes terapéuticos de anticuerpos monoclonales que puedan proporcionar nuevos tratamientos para la COVID-19 .
Generar células CHO recombinantes
Descubrir un proceso eficaz y rápido para generar líneas celulares CHO recombinantes
La selección de líneas celulares CHO de mamífero de alta producción sigue representando un importante cuello de botella en el desarrollo de procesos para la producción de productos biofarmacéuticos. Por lo tanto, es cada vez más importante desarrollar nuevos métodos de alto rendimiento para la selección de líneas celulares CHO de alta expresión de una manera eficiente y económica.
En esta nota de aplicación, descubre un proceso eficaz y rápido para generar líneas celulares CHO recombinantes, produciendo altos niveles de proteínas terapéuticas.

Los dispositivos moleculares proporcionan una solución rápida, sencilla e integral para el desarrollo de líneas celulares CHO. Cuando se combinan con el agente de detección CloneDetect, el generador de imágenes CloneSelect™ y el sistema ClonePix™ , permiten a los investigadores desarrollar con más eficiencia nuevas líneas celulares CHO productoras de proteínas, acelerando así su salida al mercado.