
[Podcast] Desafíos del desarrollo tradicional de líneas celulares y tecnologías emergentes para ayudar a regular la monoclonalidad
Los progresos en ingeniería genética y biología sintética han permitido numerosos avances en las últimas décadas. La importancia del desarrollo de líneas celulares merece una mención especial… Sin ella, muchas vacunas que salvan vidas para enfermedades infecciosas, fármacos de anticuerpos y productos de proteínas recombinantes, incluida la insulina, no estarían ampliamente disponibles. El paso más difícil del desarrollo de líneas celulares compatibles es la garantía de monoclonalidad, principalmente cuando se lleva a cabo manualmente. La monoclonalidad de las líneas celulares terapéuticas debe lograrse y documentarse por motivos normativos.
En nuestro podcast, “Desarrollo de líneas celulares con la Dra. Natasa Skoko, ICGEB y el Dr. Hugh Graham, MacroGenics”, analizamos los flujos de trabajo tradicionales para el desarrollo de líneas celulares y las tecnologías emergentes para ayudar a verificar la monoclonalidad.
Aquí hemos resumido los puntos clave de debate de los ponentes expertos: La Dra. Natasa Skoko, líder de grupo de la Unidad de Desarrollo Biotecnológico del Centro Internacional de Ingeniería Genética y Biotecnología (International Centre for Genetic Engineering and Biotechnology, ICGEB), y el Dr. Hugh Graham, director de Ciencias de Cultivos Celulares en MacroGenics.
Desarrollo de líneas celulares
Garantía de monoclonalidad
Tecnologías emergentes e impacto normativo
Significado de las líneas celulares estables
En la forma más simple, el término línea celular define una población de células que pueden mantenerse en un cultivo durante un determinado período y retener un fenotipo, función y estabilidad distintos.
El Dr. Skoko resume la importancia histórica de la línea celular estable. “El uso de la línea celular hizo la revolución, no solo en la investigación científica y ayudó a comprender muchos procesos biológicos fundamentales”, Sus aplicaciones van desde la producción de anticuerpos y proteínas terapéuticas hasta el cribado de fármacos.
El desarrollo de líneas celulares implica células de mamíferos modificadas genéticamente que son robustas, rentables y fáciles de cultivar. Una línea celular que cumple todos los criterios es la célula de ovario de hámster chino (CHO), desarrollada por primera vez en 1987. Hoy en día, el 70% de los bioterapéuticos del mercado se fabrican a partir de líneas celularesCHO. Son particularmente eficientes en la producción masiva de bioterapéuticos, gracias a su adaptabilidad a diversos medios de crecimiento y condiciones de crecimiento (por ejemplo, suspensión, crecimiento unido, lote alimentado, perfusión), así como a su capacidad de doblar y glicosilar proteínas para imitar modificaciones postraduccionales en proteínas humanas.
Desafíos de un flujo de trabajo de desarrollo de líneas celulares tradicional
La producción de altos niveles de bioterapéuticos depende de la generación de líneas celulares estables.
La primera etapa es la transfección de una línea celular huésped adecuada con el gen de interés, lo que conduce a la integración aleatoria del ADN en el genoma huésped. Una vez que la línea celular modificada genéticamente comienza a crecer, normalmente bajo presión de selección, se necesita aislamiento de una sola célula para generar clones para el cribado.
En los flujos de trabajo tradicionales, las células se sembran en una placa 96de pocillos a través de la dilución limitante. Este método implica la dilución de la suspensión celular de manera que cuando se coloca una cierta cantidad en un pocillo, la probabilidad de que solo tenga una célula es muy alta. Algunos pocillos pueden incluso estar vacíos y algunos pueden tener varias células. Por lo tanto, tiene una alta probabilidad de que una línea celular de cualquiera de estos pocillos se desarrolle a partir de una sola célula.
Esto es genial, pero ¿cuánto tiempo lleva? Suponiendo que las células se duplican en números cada 24 horas, se tarda diez veces en alcanzar mil células, lo que tardaría 10 días. Para obtener suficientes células con las que trabajar, tardaría 2entre y3 semanas. Además, las normativas de monoclonalidad requieren que repita la dilución limitante para garantizar aún más el origen clonal de su línea celular. Por lo tanto, tendría que pasar meses para obtener resultados de este método de bajo rendimiento. El Dr. Graham añade: “La estabilidad de la línea celular es un desafío. Para cuando llegue a los números deseables y tenga una alta garantía de monoclonalidad, existe la posibilidad de que se hayan desviado de sus propiedades, perdido algunas copias del gen de interés o adaptado de una manera que usted no esperaba”.
En resumen, la limitación de la dilución puede no lograr la velocidad, el cumplimiento y la calidad de la línea celular porque es difícil documentar la monoclonalidad y conservar la calidad de sus células. Tanto el Dr. Skoko como el Dr. Graham coinciden en que la automatización es la forma de facilitar el crecimiento de la línea celular monoclonal de alto rendimiento y su documentación.
Fundamentos de la línea celular monoclonal
Vamos a dar un paso atrás para definir la monoclonalidad. Una línea celular monoclonal se origina a partir de una sola célula o de un único progenitor.
¿Por qué es tan importante? A medida que las células comienzan a crecer y duplicarse, están sujetas a desviaciones genéticas, mutaciones o pérdida de un plásmido. Por lo tanto, es casi imposible garantizar que la calidad de las proteínas terapéuticas que expresan sea uniforme simplemente investigando su fenotipo más reciente.
Para compensarlo, debe comenzar a documentar sus células el día cero para demostrar que, de hecho, provienen de una sola célula.

El crecimiento celular de CHO-s se utilizó para capturar imágenes de las placas 6de pocillos en múltiples puntos temporales. El día 0, se observa claramente en la fila superior que hay una celda presente mientras que en la fila inferior se observan dos celdas. El círculo amarillo muestra la posición de una microesfera que sirve como referencia de ubicación para confirmar que se obtienen imágenes de la misma colonia con el tiempo.
Las pruebas de monoclonalidad típicas que buscan los reguladores se basan en imágenes, es decir, se debe registrar la imagen de una sola célula.
El equipo de desarrollo de líneas celulares monoclonales más eficaz es una impresora de células individuales, que realiza el depósito de células individuales. Otros métodos incluyen la clasificación celular activada por fluorescencia (FACS) y flujos de trabajo que automatizarán cada paso, desde la incubación hasta el pipeteo.
Importancia de verificar la monoclonalidad temprana
La garantía de monoclonalidad en una fase temprana tiene varias implicaciones para las aplicaciones de las ciencias biológicas. El Dr. Graham destaca la importancia de la monoclonalidad para el ciclo de desarrollo del fármaco: “Hay líneas celulares y moléculas que se destinan a la comercialización que se desarrollaron hace diez años o más. Los procesos de clonación de hace diez años pueden no tener la documentación necesaria para garantizar un origen clonal. Cuando se lleva una línea celular de este tipo a un regulador, es posible que se le pida que muestre que originalmente provenía de una línea celular clonal. Si no tiene esa prueba, entonces probarla más adelante en el proyecto es mucho trabajo”.
El Dr. Skoko añade: “Se trata de minimizar el riesgo y tener un proceso de producción y una calidad del producto coherentes. Por eso es esencial garantizar la monoclonalidad en la fase temprana. Empezar con un banco de células con una alta garantía de monoclonalidad da como resultado menos trabajo más tarde. Además, evitará graves interrupciones en la fabricación y reducirá la incertidumbre al realizar cambios en el proceso de fabricación”.
Tecnologías monoclonales emergentes para verificar líneas celulares únicas
Las técnicas emergentes para la obtención y el cultivo de imágenes de líneas celulares monoclonales están creciendo. Estos son algunos ejemplos:
- La suspensión de células semisólidas, mediante la cual una sola célula crece en una suspensión semisólida, se puede obtener una imagen a medida que crece.
- Un anillo de clonación que rodea una sola célula para aislarla y protegerla de la contaminación
- FACS: La clasificación de las células en función de las características fluorescentes
- Impresoras monocelda microfluídicas basadas en gota con la capacidad de obtener imágenes de pocillos recién bañados que contienen células individuales
Estos métodos combinados mejoran la credibilidad de las pruebas de monoclonalidad.
Por supuesto, existe un gran potencial para mejorar las técnicas actuales e inventar técnicas superiores. En primer lugar, la evidencia visual, es decir, la obtención de imágenes unicelulares, debe utilizarse con más frecuencia, ya que supera los desafíos relacionados con el coste y el tiempo de limitar la dilución y la clasificación por citometría de flujo.
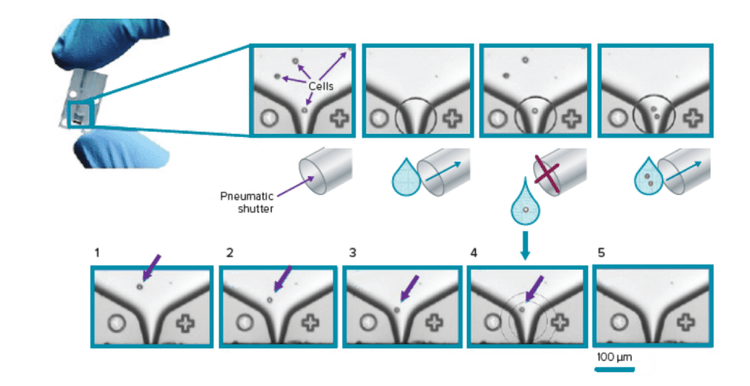
La serie de impresoras de una celda CloneSelect es un sistema totalmente automatizado que utiliza tecnología patentada basada en microfluidos y análisis de imágenes en tiempo real para clasificar y depositar células individuales en microplacas estándar, al tiempo que proporciona simultáneamente garantía de monoclonalidad a través de la documentación de imágenes.
Es posible realizar más mejoras en la línea de producción. Por ejemplo, la mejora de los métodos analíticos en la producción de proteínas terapéuticas puede ayudarnos a supervisar todo el proceso de fabricación. Esto controla la variación genética y garantiza la uniformidad de la proteína fabricada.
Otra preocupación en el desarrollo de líneas celulares monoclonales es la velocidad. Como señala el Dr. Graham: “Esperar a que una línea celular clonal produzca su proteína para ir a una clínica es una barrera en términos de tiempo. Hoy en día, las personas se están acercando a los primeros lotes de proteínas de grupos de clones tempranos para el primer material clínico de Buena Práctica de Fabricación (BPF). A continuación, se genera la línea celular clonal para ensayos clínicos en etapas posteriores y la producción de BPF. Eliminar la necesidad de pruebas de origen clonal en los primeros ensayos clínicos es un enfoque interesante para acelerar el desarrollo bioterapéutico. Sin embargo, este enfoque puede necesitar trabajo adicional para obtener la aprobación regulatoria”.
El papel de la regulación y su impacto en el proceso de desarrollo de líneas celulares
Como puede ver, las normativas innegablemente afectan al desarrollo de la línea celular monoclonal. Una implicación de las estrictas normativas es que el fabricante debe proporcionar un informe completo sobre la línea celular monoclonal antes de solicitar la aprobación. Una prueba insuficiente o la falta de documentos pueden provocar retrasos normativos o compromisos adicionales posteriores a la aprobación. Dado que la aprobación reglamentaria requiere un excelente apoyo científico, es mejor proporcionar tanta prueba desde las primeras etapas como sea posible, especialmente para el origen clonal.
¿Qué depara el futuro para los flujos de trabajo de líneas celulares monoclonales?
Existen desafíos no resueltos en los flujos de trabajo de líneas celulares monoclonales, incluidas las preocupaciones financieras, la obtención de resultados de alto rendimiento y la garantía de origen monoclonal.
En comparación con los métodos heredados, los desarrolladores de líneas celulares monoclonales de hoy en día tienen herramientas mucho mejores para garantizar el cumplimiento normativo y la calidad de las líneas celulares.
Una perspectiva emocionante es la mejora de la gestión de datos, que es necesaria para organizar grandes conjuntos de datos generados a partir de estudios de desarrollo de líneas celulares. La combinación de la gestión de datos con el aprendizaje automático puede dar lugar a una plataforma que predice la calidad de un bioterapéutico basándose únicamente en el origen clonal.
El papel de la automatización también será más fundamental en velocidad y consistencia. Más específicamente, la automatización puede acelerar el desarrollo de clones y el cribado de colonias. El Dr. Skoko aclara los efectos de la automatización: “Estamos hablando de la detección de 10 000 clones en un par de semanas. Un flujo de trabajo tradicional tardaría entre 30 semanas y dos años. La tecnología automatizada puede ayudarnos a tener clones precisos, eliminar errores asociados con la dilución limitante tradicional y superar el trabajo con una población heterogénea de diferentes secretores. Puede evaluar la estabilidad de sus clones desde el principio”.
Flujo de trabajo automatizado de desarrollo de líneas celulares con garantía de monoclonalidad
Con la integración de las tecnologías de automatización, puede filtrar cientos de miles de clones para encontrar ese clon dorado que puede generar el mayor rendimiento para la proteína de su interés. Y lo que es más importante, te ayuda a documentar completamente cada paso del proceso de desarrollo desde el día cero. En última instancia, puede ahorrar dinero y tiempo evitando futuros conflictos causados por una falta de garantía de monoclonalidad o una calidad de producto inconsistente.
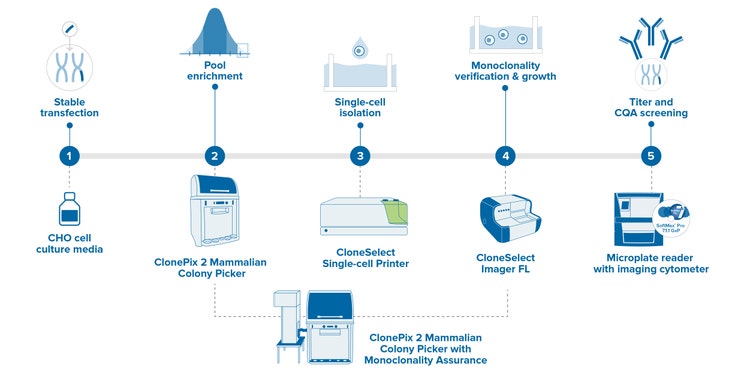
Acelere sus plazos de desarrollo de líneas celulares integrando múltiples pasos en un solo paso. El Selector de colonias de 2 mamíferos ClonePix mejorado con garantía de monoclonalidad puede detectar y seleccionar automáticamente clones de alta producción y monoclonales, todo en un solo sistema. Realice cribados de más clones en menos tiempo con verificación de monoclonalidad el día cero y, a continuación, cribe y seleccione los clones más productores en menos de dos semanas. La función de adquisición Z-stack rápida permite la detección de células individuales a través del volumen del medio, no solo en un único plano focal, el día .

Molecular Devices cuenta con una sólida cartera para automatizar su flujo de trabajo de desarrollo de líneas celulares y tecnologías para garantizar la monoclonalidad, incluida la selección de clones, el aislamiento y la obtención de imágenes de células individuales y los lectores de microplacas. Nuestras soluciones GxP probadas ayudan a garantizar la integridad y el cumplimiento de los datos para laboratorios GMP/GLP.
Obtenga más información sobre el desarrollo de líneas celulares y las aplicaciones de monoclonalidad o hable con un especialista en automatización si está interesado en explorar una solución automatizada para su laboratorio.